-
01-29 21:10...该款猴痘疫苗于2024年9月9日,获得国家药品监督管理局签发的临床试验通知书,是我国首款获批临床的猴痘疫苗,有望在我国对猴痘病毒导致疾病的预防和控制中发挥重要作用。1月22日,MVA株猴痘减毒活疫苗I期临床首批受试者完成入组,标志着我国首款猴痘疫苗正式迈入临床试验阶段。该临床将在不同人群中充分评价疫苗的安全性与免疫原性... 0
-
01-28 15:40...办理3个体外诊断试剂产品的临床试验备案。在厦门工作站工作人员确认其递交的纸质资料没问题后,他便离开了。当天下午,高磊接到领证通知,并顺利拿到了产品的临床试验备案表。“之前,我们都是到福州办理备案事项。要么出差,要么把材料邮寄过去,需要一周左右才能拿到盖章的备案表。有了厦门工作站之后,只要材料符合要求,我们最快当天即可完... 0
-
01-23 13:40...中国公司获得了60亿美元的许可预付款,在环球经贸吹逆风下,成为中西合作难得的亮点。根据国家药品监督管理局新药审评机构药物审评中心的数据,仅在2022年至2023年期间,中国的临床试验注册数量激增了26%以上,而且过去五年临床试验的数量一直呈上升趋势,中国成了推进全球生物技术创新的一个重要引擎。从小型生物技术公司收购资产... 1
-
01-19 11:00...IgA肾病适应症(IgAN)国内Ⅲ期临床试验已完成患者入组,预计2025年上半年读出36周的数据。据弗若斯特沙利文报告,全球IgAN患者约1020万人,包括中国237万,预计2030年全球市场规模为25亿美元。干燥综合征适应症(pSS)国内Ⅲ期临床试验顺利推进,预计2025年上半年读出24周的数据。据弗若斯特沙利文报告... 2
-
01-19 06:50...2025年1月13日,该新药正式获得国家药品监督管理局批准,可开展用于高脂血症的临床试验,标志着在抗高脂血症中药新药研发领域迈出了重要一步。在新药研发过程中,市中药研究院依托中药药理与毒理学科及重庆市药物安全评价中心(GLP中心)的基础优势,完成了多项合作研究,包括“苦丁茶总皂苷大、小鼠安全性评价研究”“苦丁茶总皂苷片... 1
-
01-19 03:30...黄仁勋出席了今年的JPM大会,并与基因测序公司因美纳(Illumina)、顶级医疗机构妙佑国际医疗(MayoClinic)等行业企业高管讨论AI如何改变生物医学研究、临床试验和病理学。黄仁勋在大会的一场炉边对话中扮演了一位深夜脱口秀主持人的角色,他逐一打电话给几位演讲嘉宾,询问他们如何利用AI技术创新加速生物医学研究的... 0
-



-
01-19 02:40...Intra-Cellular的身家性命几乎完全依赖于lumateperone的进展。但lumateperone的研发耗时极为漫长,这也使得Intra-Cellular的股价长期低迷。时间一晃来到2019年10月,Intra-Cellular股价跌至6.75美元,创下了上市后的最低点,比发行价还低一半。在此之前,luma... 1
-
01-18 02:30...这是深圳医疗机构与本土医疗器械企业的一次深度融合探索,项目的开展将有效整合更多优质医疗资源,进一步推动深圳整体医疗水平提升,为更多患者带来福音。据了解,远程手术为医疗资源的合理分配、偏远地区患者的精准治疗乃至整个医疗服务体系的优化带来颠覆性意义。通过远程手术,医生可以不受地域限制,实时操控手术机器人进行手术操作,实现医... 1
-
01-12 02:40...在部分地区开展优化创新药临床试验审评审批试点,将审评审批时限由60个工作日缩短为30个工作日。医疗器械临床试验审评审批时限也由60个工作日缩短为30个工作日。有利于药械企业加速临床试验,促进产品尽快上市。加强知识产权保护,鼓励药品医疗器械研发。对于广大医药企业而言,创新药械研发的风险高、投资大、周期长,加强知识产权保护... 1
-
01-11 15:00...有投资者在投资者互动平台提问:六价诺如病毒疫苗临床后要多久可以批量生产2025-01-10六价诺如病毒疫苗,康华生物,公司界面新闻记者庄键瑞浦兰钧(00666.HK)首座海外电池工厂正式官宣。1月9日晚间,瑞浦兰钧公告称,将在印度尼西亚建立电池工厂,该工厂将从事锂电池、组件、模组以及电池包的研发、制造和销售,瑞浦兰钧并... 1
-
01-11 11:00...10家以上产业链上下游国内骨干企业。脑机接口创新生态初步构建。2030年前,实现高质量控脑,脑机接口产品全面实现临床应用,打造全球脑机接口产品创新高地,产业链核心环节实现自主可控,脑机接口产业发展成为战略性新兴产业中坚力量。加快脑机接口产品化《行动方案》充分发挥上海产业配套支撑条件好、临床资源丰富等优势,推进产品研发。... 3
-
01-11 04:30...研究团队就试验实施中可能遇到的问题和解决方案进行了充分的讨论。该项目针对EGFR表达的晚期不可切除或转移性实体瘤患者的药物临床试验,主要目的是评价SYS6010单药或联合SYH2051治疗EGFR表达的晚期实体瘤患者(包括但不限于乳腺癌)的安全性和耐受性,从而为医生和患者提供更多治疗选择和依据。该项目的实施有助于提升医... 1
-



-
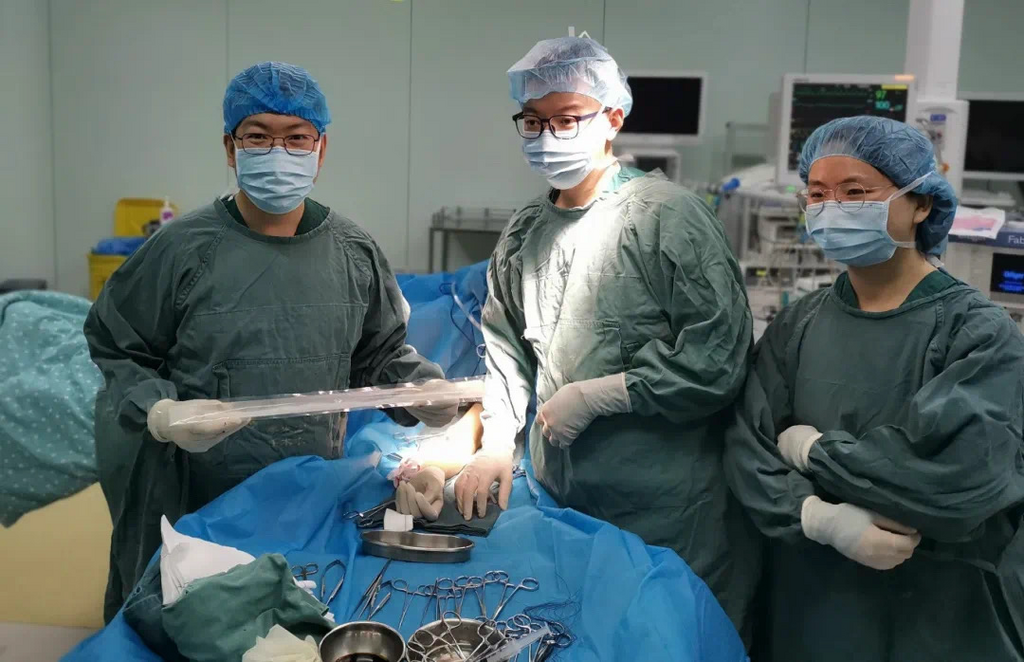
01-09 02:30...重医附一院血管外科专家为李大爷进行手术。重医附一院供图1月8日,记者从重医附一院获悉,重医附一院金山院区尿毒症患者李大爷在接受一项临床试验2年后,人工血管竟然“蜕变”成真正属于他的自体血管,这在全球尚属首例。据悉,今年70岁的李大爷家住重庆北碚区,7年前被确诊为尿毒症,每周要做约3次血液透析治疗。2022年,李大爷手上... 7
-
01-08 22:50...临床试验批件为公司与军科院共有(具体内容详见公司于2015年8月6日刊登在中国证券报、上海证券报、证券时报、证券日报及上海证券交易所网站www.sse.com.cn上的《浙江华海药业股份有限公司关于获得创新药盐酸羟哌吡酮临床批件的公告》(公告编号:临2015-062号))。本次挂牌转让价格由公司与军科院在评估双方享有权... 4
-
01-07 18:10...66E,智算占比超过30%,而算力规模每增长1个百分点,预计可带动GDP增长0.2个百分点。“推出算力券奖补是很有激励性的实招,将有效带动企业深挖算力潜能,降低应用成本,并引导更多行业积极引入人工智能算力,提升整体运营效率与经济效益。”山东省计算中心(国家超级计算济南中心)工程师张镇指出。记者从省大数据局获悉,省级财政... 9
-
01-06 02:30...完善药品医疗器械知识产权保护相关制度。部分药品获批上市时,对注册申请人提交的自行取得且未披露的试验数据和其他数据,分类别给予一定的数据保护期。对符合条件的罕见病用药品、儿童用药品、首个化学仿制药及独家中药品种给予一定的市场独占期。加快药品医疗器械原创性成果专利布局,提升专利质量和转化运用效益。(国家知识产权局、国家药监... 2
-
01-05 18:20...至今仍无商业化产品,属于无产品、无收入、无利润的“三无公司”。成立至今,公司陷入持续亏损之中。2022年、2023年及2024年上半年,公司亏损额分别为2.52亿元、3.43亿元、1.6亿元。截至2024年6月30日,公司累计亏损已达12.85亿元。由于没有自主造血能力,药捷安康长期依靠外部融资输血维持经营。截至招股书... 2
-
01-05 02:10...通常与大脑的复杂认知功能和神经活动同步有关,它能提供大脑活动的详细信息,尤其是运动和语言相关信息。“256个记录通道,不仅仅是收集的脑电数据有了数量级增长,与之前的脑机接口技术相比,更是有了质的变化。”脑虎科技创始人陶虎说。据介绍,得益于256导高通量、高质量、高分辨脑电信号和自主开发的通道筛选算法,可快速精准定位脑区... 6
-



-
01-04 14:00...国务院办公厅印发《关于全面深化药品医疗器械监管改革促进医药产业高质量发展的意见》(下称《意见》)。《意见》明确5方面24条改革举措。一是加大对药品医疗器械研发创新的支持力度。二是提高药品医疗器械审评审批质效。三是以高效严格监管提升医药产业合规水平。四是支持医药产业扩大对外开放合作。五是构建适应产业发展和安全需要的监管体... 3
-
11-04 02:20...不仅对发展国家医药事业、保障人民健康、惠及广大患者有着重要意义,而且有利于提升医院各专业科室研究者的学术水平、专业能力,从而提升医院层次,全面加快医院发展步伐。药物临床试验现场检查会议。通讯员供图自2021年05月,医院成立药物临床试验管理机构以来,院党委高度重视药物临床试验管理规范(GCP)软硬件、人员、体系等建设工... 4
-
11-03 23:40...公司没有涉及减肥功效产品的收入。“没有涉及减肥功效产品的收入”在异动公告中,常山药业提示,公司开展的艾本那肽临床试验,适应症为治疗2型糖尿病,不涉及肥胖适应症。公司尚未开展艾本那肽针对肥胖或减重的临床试验;没有涉及减肥功效产品的收入。常山药业还称,目前艾本那肽注射液尚未上市销售。公司已经完成艾本那肽临床试验,尚未向国家... 1
-
11-03 22:00...2023年2月,由中国中医药循证医学中心建设的国际传统医学临床试验注册平台正式被世界卫生组织临床试验注册平台接受为一级注册机构。这是世界上首个跨国家和地区的以临床试验为主题范围划分的注册机构,是中医药乃至全球传统医学临床科研规范化、国际化发展的重要渠道。”黄璐琦说,“国际传统医学临床试验注册平台将为提升全球传统医学临床... 1
-
-
-
本页Url:
-
2025-01-30-05:47 GMT . 添加到桌面浏览更方便.
-